Применение L-аргинина в акушерской практике (обзор литературы)
Клінічні та експериментальні дослідження
Применение L-аргинина в акушерской практике (обзор литературы)
В настоящее время имеются многочисленные данные о роли дисфункции эндотелия в патогенезе таких осложнений при беременности, как привычное невынашивание, плацентарной дисфункции (ПД), синдром задержки развития плода (СЗРП), поздний гестоз. Дисфункция эндотелия, развивающаяся у беременных, страдающих сахарным диабетом, гипертонической болезнью, аутоиммунными заболеваниями, приводит к нарушению микроциркуляции в плаценте и препятствует нормальному течению беременности[1,3,6,8,9,10,11,14,21,24]. При физиологической беременности наблюдаются стимуляция и активация фетоплацентарного комплекса, что приводит к возрастанию коагулянтного потенциала почти в 2 раза увеличивается содержание всех факторов свертывания на фоне снижения фибринолитической и антикоагулянтной активности. Начиная со II триместра беременности отмечается повышение продукции эндотелием и секреции в кровь фактора Виллебранда, тромбоксана, эндотелина-1, тромбомодулина и фибронектина, что позволяет высказать предположение о формировании синдрома эндотелиальной дисфункции в фетоплацентарном комплексе даже при физиологическом течении беременности[1,6,22]. Эндотелий – это не просто слой клеток, а отдельный эндокринный орган, самый крупный в организме, от нормального функционирования которого зависят важнейшие системы организма.
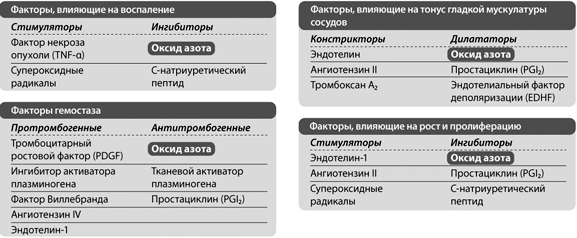
Эндотелий — внутренняя выстилка сосудов, выполняющая различные функции[1,11,16,22]:
- регуляция тонуса сосудов (синтез вазоактивных медиаторов),
- поддержание их анатомического строения (синтез и ингибирование факторов пролиферации),
- сохранение гемостаза (синтез и ингибирование факторов фибринолиза и агрегации тромбоцитов);
- участие в процессах местного воспаления (выработка про- и антивоспалительных факторов).
В норме антикоагулянтная и антитромботическая способность эндотелия преобладает над его прокоагулянтными свойствами. Однако под действием повреждающих факторов изменяется фенотип эндотелиального слоя и проявляется его прокоагулянтная активность. Повреждение эндотелия может быть результатом воздействия различных факторов: механической травмы сосудов, воздействия провоспалительных цитокинов, эндотоксинов и других компонентов клеточной стенки бактерий, иммунных комплексов, атерогенных стимулов (липопротеины низкой плотности, гомоцистеин)[3,11,13,21].
Эндотелиальная дисфункция отражает генерализованное нарушение всех функций эндотелия, что сопровождается нарушением регуляции сосудистого тонуса, проницаемости, увеличением прокоагулянтной, проагрегантной, антифибринолитической и противовоспалительной активности эндотелиального слоя[2,4,18,19].
Процесс имплантации, инвазии трофобласта и дальнейшее успешное функционирование плаценты являются сложным процессом эндотелиально-гемостазиологических взаимодействий со сложной регуляцией, который объективно нарушается при тромбофилии и сахарном диабете и часто приводит к развитию гестоза, ПД, СЗРП [1,8,9,10,11,16,22].
Нарушение процессов инвазии трофобласта не приводит к физиологической перестройке спиральных артерий, и они остаются чувствительными к патологическим изменениям гемодинамики материнского организма. Прогрессирование беременности в таких условиях ведет к нарушению плацентарной перфузии и формированию последующих осложнений — гестоза, ПД, СЗРП, преждевременной отслойки нормально расположенной плаценты (ПОНРП), гипоксии плода, дистресса плода. Важное значение отводится недостаточному синтезу простациклина (PGI2) в трофобласте, фетоплацентарном комплексе и пупочных артериях. Это приводит к отложению фибрина и развитию эндотелиоза клубочков почек, а также развитию ДВС-синдрома[5,19].
Гестоз является наиболее сложной патологией в акушерстве. D.A. Davey отмечает, что гестоз наблюдается в 2,3-28,5% случаев, и этот показатель не имеет тенденции к снижению [17]. При высоком уровне медицинских технологий в мире ежегодно умирает около 50 тыс. женщин от причин, связанных с беременностью и родами. К сожалению, несмотря на современные успехи в профилактике, диагностике и лечении, перинатальная смертность при гестозе в 3-4 раза превышает популяционную и составляет от 18 до 30%. Перинатальная заболеваемость также не имеет устойчивой тенденции к снижению.
Преэклампсия осложняет течение от 3 до 5% всех беременностей и представляет собой основную причину материнской и перинатальной заболеваемости и смертности во всем мире [18]. Недооценка степени тяжести гестоза, а следовательно, неадекватное лечение и запоздалое родоразрешение являются основными причинами материнской смертности при данном осложнении беременности. Для беременных с гестозом характерна циркуляция в крови множества маркеров активации эндотелия, включая сниженный уровень PGI2 и оксида азота, повышенный уровень эндотелина-1, клеточного фибронектина и тромбомодулина, повышение экспрессии молекул адгезии. В условиях эндотелиальной дисфункции нарушается баланс про- и антикоагулянтных механизмов. При этом поверхность эндотелия приобретает прокоагулянтную активность. В условиях эндотелиопатии при гестозе наблюдается снижение экспрессии важнейших естественных антикоагулянтов, включая протеины C и S, антитромбина III. Важнейшую роль в дисбалансе коагуляционного каскада у беременных с гестозом играют ингибиторы фибринолиза. Так, концентрация ингибитора активатора плазминогена 1-го типа (PAI-1), синтез которого во время беременности в основном осуществляется плацентой, и PAI-2 повышается у беременных с гестозом. В ответ на повреждение или активацию эндотелиальные клетки экспрессируют гликопротеины экстрацеллюлярного матрикса с прокоагулянтной активностью, такие как фибронектин, фактор Виллебранда. Уровень PAI, тромбомодулина и фибронектина, эндотелина-1 четко коррелирует с тяжестью гестоза [1,3,5].
Эндотелиальные повреждения все чаще стали рассматриваться как важнейшие факторы разнообразных осложнений беременности, в том числе и синдрома потери плода[3,8]. В первую очередь возникают многочисленные повреждения эндотелиального покрова ворсин плаценты, что приводит к нарушению целостности щеточной каймы и повреждению синцитиотрофобласта и соответственно к нарушению функции плаценты. Дальнейшее неблагоприятное воздействие повреждающих факторов вызывает оголение базального слоя и даже стромы ворсин и высвобождение дополнительных плацентарных коагулирующих агентов (тромбоксана А2, тканевого фактора, коллагена). Обнажение коллагена базального слоя ворсин, который является мощным активатором фактора Хагемана, приводит к запуску внутреннего пути коагуляции материнской крови в межворсинчатом пространстве. Клинически это проявляется первичной или вторичной плацентарной недостаточностью, случаями замершей беременности, угрозой аборта и преждевременными родами, СЗРП, ПОНРП и другими тяжелыми осложнениями беременности и родов[5].
Основным фактором, который приводит к генерализованной дисфункции, является дефицит оксид азота (NO), который образуется в сосудистом эндотелии и является мощным вазодилятатором. Аминокислота L-аргинин — субстрат для синтеза оксида азота. Аргинин — условно незаменимая аминокислота. Средний суточный уровень ее потребления составляет 5,4 г. Он служит необходимым предшественником для синтеза белков и многих биологически важных молекул. Однако главная роль аргинина в организме человека — быть субстратом для синтеза оксида азота (NO). Физиологическая сосудистая адаптация к беременности (увеличение объема крови, минутного объема сердца и снижение сосудистой резистентности) сопровождается увеличением эндогенной продукции NO и повышением чувствительности к NO гладкомышечных клеток сосудов. Экспериментальные исследования показали роль усиления оксидативного стресса и снижения биодоступности таких вазодилататоров как NO в патогенезе сердечно-сосудистой дисфункции во время беременности[1,3,6,8,9,10,11,14,21,24].|
Эндотелиальная, или сосудистая теория возникновения таких осложнений беременности:
- Эндотелий сосудов является одним из главных факторов регуляции сосудистого тонуса, состояния микроциркуляции и всех ее составляющих
- При нормальном течении беременности происходит физиологическая интенсификация в системе L-аргинин/оксид азота, которая направлена на поддержание оптимального маточно-плацентарного кровотока.
- При эндотелиальной дисфункции (нарушении в системе L-аргинин/оксид азота) происходит генерализованный спазм сосудов с повышением периферического сопротивления и внутрисосудистыми коагуляционными нарушениями.
- Возникающая гипоперфузия тканей вследствие вазоконстрикции, гиповолемии, нарушений реологических свойств крови и гиперкоагуляции неизбежно приводит к ишемическим повреждениям в тканях различных органов, в том числе матке и плаценте.
Все перечисленное приводит к:
- уменьшению маточно-плацентарного и фетоплацентарного кровотока;
- снижению кровоснабжения плаценты и плода;
- ограничению газообмена и метаболизма в фетоплацентарном комплексе;
- нарушению процессов созревания плаценты;
- развитию дистресса плода;
- рождению детей с низкой массой тела;
- развитию ряда осложнений периода новорожденности, включая высокую детскую летальность.
Особый интерес вызывают публикации и признание медицинской общественностью в США и в странах Европы результатов исследований, в ходе которых появилась возможность достоверно прогнозировать преэклампсию за 5 нед до развития ее клинических проявлений. Так, в 1992-1995 гг. R. Levine et al. [19] провели в пяти медицинских центрах США двойное слепое рандомизированное контролируемое исследование с участием 120 здоровых женщин с первой беременностью на сроках 13-21 нед. Пациентки были обследованы в отношении определения содержания ангиогенных факторов – общего уровня растворимой fms-подобной тирозинкиназы-1 (sFlt-1), концентрации свободного плацентарного фактора роста (ПФР) и свободного сосудистого эндотелиального фактора роста (СЭФР). Как известно, sFlt-1 является эндогенным антиангиогенным белком, который вырабатывается в плаценте и нейтрализует проангиогенные белки СЭФР и ПФР. Повышение содержания сывороточных sFlt-1 (с одновременным снижением уровня свободных фракций ПФР и СЭФР) обнаружено при преэклампсии и предшествует ее развитию. Эти изменения начинаются за 5 нед до манифестации симптомов заболевания, содержание sFlt-1 составляет 4382 пкг/мл, в то время как в аналогичные сроки при нормальной беременности – 1643 пкг/мл (p < 0,001). Обратные тенденции имеют место по уровню сывороточной концентрации ПФР, которая у пациенток с последующим развитием преэклампсии снижается по сравнению с контролем уже с 13-16-й недели беременности, составляя в среднем 90 и 142 пкг/мл соответственно (р < 0,01).
По мнению A. Wikström et al., эти изменения более значительны при раннем возникновении преэклампсии и рождении ребенка с синдромом задержки внутриутробного развития [20]. K. Spencer et al. сообщают, что крайне важным элементом в прогнозировании исходов беременности при преэклампсии являются показатели кровотока при допплерометрии маточных артерий, особенно при одновременной оценке ангиогенного профиля. При диагностировании на 22-26-й неделе беременности признаков двусторонних нарушений кровотока в маточной артерии (по наличии диастолической выемки на допплерограмме) и одновременного снижения концентрации ПФР до уровня ниже 280 пкг/мл на основании результатов 3348 проспективных исследований с высокой точностью была показана возможность прогнозирования умеренной и тяжелой формы преэклампсии [21].
В литературе имеются сообщения о повышении риска развития сердечно-сосудистых заболеваний (даже со смертельными исходами) в более отдаленном будущем у женщин, перенесших преэклампсию, особенно при первых родах. В публикациях ряда стран (Норвегии, Ирландии, Шотландии, Израиля) суммарно на примере анализа исходов 800 тыс. беременностей было показано двукратное повышение риска смерти у перенесших преэклампсию пациенток, особенно при преждевременных родах [24].
Норвежские исследователи представили данные национального регистра, включавшие сведения о 636 372 родах за 1967-1992 гг., с помощью которых удалось получить представление о риске смерти от сердечно-сосудистых заболеваний в результате преэклампсии. Так, за 25 лет от этого осложнения беременности погибли 4350 женщин, среди них пропорция между перенесшими преэклампсию при срочных родах составила 6,6/1000, при преждевременных – 15,5/1000 [23].
Следует подчеркнуть, что объем профилактических мероприятий зависит от степени риска развития акушерский осложнений. В обследовании необходимо предусмотреть изучение показателей системы гемостаза, поскольку доказана высокая прямая корреляционная связь между их значениями и маркерами эндотелиальной дисфункции. Е.В. Мозговая и соавт. [6,12] считают, что выявление многих маркеров эндотелиальной дисфункции является трудоемким и дорогостоящим, однако проведение некоторых исследований, в частности определение количества десквамированных эндотелиоцитов и фактора Виллебранда, вполне доступно большинству стационаров.
Итак, согласно результатам нашего обзора, профилактику гестоза, У ПБ, ПД, ЗВУР следует проводить пациенткам с наличием
- гестоза тяжелой степени в анамнезе;
- соматической патологии с эндотелиальной дисфункцией;
- отягощенном гинекологическом анамнезе;
- наследственности в генезе гестоза (гестоз во время беременности у мамы или сестры беременной, у мамы или у предыдущей жены партнера);
- двух и более генов предрасположенности к гестозам;
- беременности наступившей вследствии ЭКО;
- использование донорских ооцитов и донорской спермы;
- суррогатное материнство;
- патологических изменений при клинико-лабораторном исследовании;
- клиники прегестоза.
В настоящее время наиболее эффективным патогенетическим методом коррекции эндотелиальной дисфункции является применение физиологического донатора оксида азота — L-аргинина, который способствуют улучшению состояния эндотелия и тем самым нормализуют кровообращение как в системном, так и в маточно-плацентарном кровотоке. Единственным препаратом L-аргинина на украинском фармацевтическом рынке в необходимой дозировке является отечественный препарат Тивортин (L-аргинин 4,2 г – 100 мл). Тивортин позволяет проводить как ступенчатую терапию для пациентки с осложненным течением беременности, так и профилактические мероприятия с помощью питьевой формы – Тивортин аспартат (L-аргинин 1 г – 5 мл). [7,8,9,10,11,24].
Показано отсутствие тератогенного эффекта данного препарата, что позволяет его применять на ранних сроках беременности[1,7,24] . Назначение L-аргинина в сроке с 10 по 37 неделю беременности предупреждает развитие гипертонических состояний, снижение на 79,2% возникновения преэклампсии, снижение признаков внутриутробной гипотрофии на 16% и частоты снижения дистресса плода на 10%, снижение частоты преэклампсии средней степени с 16% до 0%, снижение угрозы преждевременных родов в 3 раза, уменьшение % прерывания беременности на ранних сроках на 12%, снижение частоты развития ЗВУР в 4 раза, нормализация показателей доплерометричекого исследования маточно-плацентарного кровотока [1,7,8,9,10,24].
Таким образом, высокая клиническая эффективность применения Тивортина и Тивортина аспартат с целью коррекции дисфункции эндотелия и профилактики осложненного течения беременности делает его перспективным для более широкого использования в акушерской практике.
Oпубикованo в Клінічні та експериментальні дослідження
Кардіопротекторний ефект донатора оксиду азоту в пацієнтів з артеріальною гіпертензією
Резюме: Останнє десятиліття ознаменувалося інтенсивним розвитком фундаментальних та клінічних досліджень щодо ролі судинного ендотелію в ґенезі серцево-судинних захворювань (ССЗ). Сьогодні увага дослідників прикута до вивчення ролі дисфункції ендотелію (ДЕ) в патогенезі ССЗ, а також до пошуку способів її ефективної корекції. В статті наводяться дані міжнародних і українських публікацій щодо можливого кардіопротекторного ефекту донатора оксиду азоту […]
ЗДОРОВ’Я НЕФРОНА — ЗАПОРУКА СТАБІЛЬНОГО АРТЕРІАЛЬНОГО ТИСКУ
Хронічна хвороба нирок (ХХН) є однією з найбільш поширених проблем у системі охорони здоров’я з тяжкими соціальними й економічними наслідками. Ця гетерогенна група захворювань об’єднує будь-які порушення нормальної структури й функції нирок з подальшим виникненням ниркових і позаниркових розладів, що мають несприятливий вплив на більшість систем організму. Важливою проблемою в усьому світі на сьогодні є […]
