Эндотелиальная дисфункция: что необходимо знать практическому врачу?
Эндотелиальная дисфункция: что необходимо знать практическому врачу?
В течение прошлых десятилетий стало очевидно, что сосудистый эндотелий ответствен за все, что происходит внутри сосуда: регулирование тонуса сосудистой стенки, поддержание суспензионной стабильности крови, обеспечение баланса локальных воспалительных, свободнорадикальных, метаболических и пролиферативных реакций. Но самое интересное и важное состоит, пожалуй, не в полифункциональности эндотелия, а в том, что он сам регулирует все «за» и «против», «больше»–«меньше». Для обеспечения каждого процесса эндотелий вырабатывает вещества, отвечающие за диаметрально противоположные эффекты, например тканевой активатор плазминогена и ингибитор тканевого активатора плазминогена, факторы роста сосудов и ингибиторы факторов роста сосудов, провоспалительные цитокины и противовоспалительные цитокины (рис. 1).
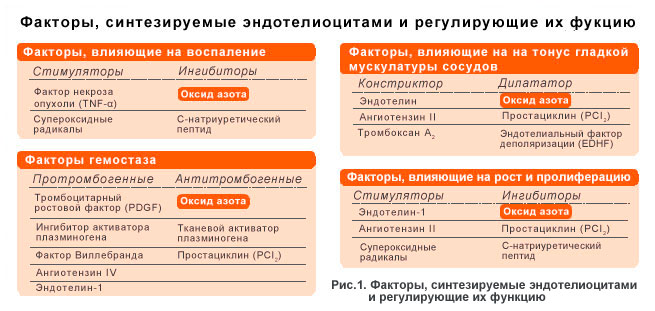
Поэтому в функционировании эндотелия наиболее важен баланс, который может обеспечить только здоровый, неповрежденный орган.
К сожалению, сегодня абсолютно очевидно, что здорового эндотелия у пациентов с заболеваниями сердечно-сосудистой системы нет. Доказано, что ЭД – основной патогенетический механизм развития и прогрессирования этой патологии, причем данное положение подразумевает и первичную ЭД (в результате воздействия внешних (стрессы, курение, несбалансированное питание, злоупотребление алкоголем и т. д.) или внутренних (генетически обусловленное нарушение метаболизма и т. д.) факторов), и вторичное поражение эндотелия в результате острых или хронических заболеваний внутренних органов либо регуляторных нарушений, оказывающих токсическое влияние на эндотелий. При этом наибольшая опасность длительного воздействия повреждающих факторов на эндотелий состоит именно в разбалансировке, нарушении соотношения про-и антисубстанций.
Эндотелиоциты относятся к числу постоянно обновляющихся клеток, то есть эндотелий при длительном воздействии повреждающих факторов не погибает, а продолжает активно бороться за поддержание стабильности внутрисосудистого гомеостаза. Но при этом в сложившихся неблагоприятных условиях (активации свободнорадикального окисления, воспаления, воздействия модифицировнных липопротеидов, избытка глюкозы, эндотоксинов и т. д.) постоянно востребуются преимущественно субстанции, обеспечивающие релаксацию сосуда, профилактику тромбообразования, противовоспалительную и антиоксидантную активность. В конечном итоге запас этих субстанций истощается и возникает дисбаланс с относительным преобладанием вазоконстрикторных, протромбогенных, провоспалительных эндотелиальных факторов, что и подтверждают результаты многочисленных исследований, посвященных изучению функционального состояния эндотелия при различных заболеваниях.
Оксид азота – «лицо» эндотелия
Когда заходит речь об эндотелии, именно оксид азота становится наиболее частым объектом внимания врачей и исследователей. Действительно, эта короткоживущая молекула, даже не молекула, а радикал, существующий в свободном состоянии несколько секунд, по сути своей является «лицом» эндотелия, поскольку в поддержании сосудистого гомеостаза обеспечивает:
– регуляцию сосудистого тонуса;
– ингибирование адгезии, агрегации тромбоцитов и
тромбообразования;
– регуляцию пролиферации и апоптоза;
– регуляцию оксидативных процессов;
– ингибирование лейкоцитарной адгезии.
Причем NO осуществляет регулирование всех этих процессов со знаком «+», то есть оказывает защитно-позитивное влияние на все перечисленные функции, а значит, относится к числу наиболее востребованных в условиях патологии субстанций.
Поэтому основным проявлением эндотелиальной дисфункции является нарушение биодоступности NO.
Обзор фармакологических средств
Врачи, как правило, сталкиваются с пациентами, у которых последствия ЭД стали уже симптомами сердечно-сосудистых заболеваний. Рациональная терапия должна быть направлена на устранение этих симптомов (клиническими проявлениями ЭД могут быть вазоспазм и тромбоз).
Так как до недавнего времени отдельного класса эндотелиопротекторных препаратов не существовало, в качестве средств, способных корригировать ЭД, рассматривали другие классы лекарственных средств, обладающих плейотропными эффектами.
Основные классы препаратов, обладающих эндотелиопротекторным действием:
–заместительные органические протективные эндотелиальные вещества (аналоги простациклина и нитровазодилататоры);
–стимуляторы синтеза эндотелиальных вазодилататоров (ингибиторы ангиотензинпревращающего фермента (АПФ), ингибиторы фосфодиэстеразы, небиволол);
– ингибиторы или антагонисты эндотелиальных вазоконстрикторов (антагонисты кальция, антагонисты рецепторов ангиотензина II, ингибиторы рецепторов эндотелина, ингибиторы тромбоксансинтетазы и тромбоксана);
– антиоксиданты;
– мембранопротекторы (статины, омега-3-полиненасыщенные жирные кислоты, эссенциальные фосфолипиды).
Остановимся подробнее на особенностях эндотелиопротекторного эффекта приведенных препаратов с учетом их потенциальных ресурсов по восстановлению функциональных возможностей эндотелиоцитов.
К первому классу предлагаемой классификации относятся заместительные органические протективные эндотелиальные вещества (аналоги простациклина и нитровазодилататоры); это самый «проблемный» класс для практических врачей.
Аналоги простациклина
Хорошо известно, что аналоги простациклина – это в основном инфузионные препараты. Их введение возможно только в стационаре и по строгим показаниям, поэтому отнести их к классу протекторных препаратов для практического применения достаточно сложно.
Нитровазодилататоры
Нитропрепараты – хорошо известная, широко применяемая группа лекарственных средств, однако их использование в качестве эндотелиопротекторов крайне нежелательно.
Во-первых, любое введение готовой заместительной субстанции приводит не к стимулированию, а к дальнейшему подавлению функции органа (это очевидно и хорошо известно на примере любых заместительных препаратов).
Во-вторых, нитропрепараты способствуют образованию пероксинитрита, который вызывает повреждение ДНК и мутации. В высоких концентрациях пероксинитрит очень токсичен: индуцирует апоптоз, нарушает функционирование системы простациклинсинтетазы, индуцирует окисление липопротеидов низкой плотности, ингибирует активность эндотелиальной NO-синтетазы.
Длительный прием нитропрепаратов и связанная с этим стабильная вазодилатация по механизму обратной связи может стимулировать нейрогуморальную активность ренин-ангиотензиновой и симпатоадреналовой систем, что крайне нежелательно для пациентов с заболеваниями сердечно-сосудистой системы.
Кроме того, длительный прием нитропрепартов истощает запас SH-групп, посредством которых реализуется эффект NO, и может блокировать работу этой системы.
Таким образом, применение нитропрепаратов, рекомендованных отдельным категориям пациентов с ИБС, для профилактики и лечения ЭД нецелесообразно.
Два следующих класса эндотелиопротекторов – стимуляторы синтеза эндотелиальных вазодилататоров и ингибиторы/антагонисты эндотелиальных вазоконстрикторов – вполне могут использоваться с эндотелиопротекторной целью.
Однако следует помнить, что ингибиторы выработки эндотелиальных вазоконстрикторов не улучшают функцию эндотелия, а только способствуют относительному сбалансированию соотношения эндотелиальных вазоактивных веществ на более низком уровне. Использование препаратов, направленных на стимулирование выработки оксида азота, зачастую не дает ожидаемого эффекта из-за истощения субстрата. По этой же причине мы можем не достичь желаемого и при применении мембраностабилизаторов, хотя эффективность статинов в качестве препаратов с доказанной эндотелиопротекторной эффективностью неоспорима.
Таким образом, применения препаратов, которые стимулируют истощенный эндотелий недостаточно, крайне важно предоставить субстрат, из которого эндотелий может синтезировать требуемые вещества. Поэтому возникла необходимость в новом классе эндотелиопротекторных препаратов, которые не только стимулируют эндотелий, но и поставляют ему субстрат.
Тивортин® – незаменимый донатор оксида азота
Почему же недостаток субстрата является настолько важным препятствием на пути стабилизации функционального состояния эндотелия и как его преодолеть?
Рассмотрим эту проблему на примере синтеза оксида азота.
Напомним, что единственным субстратом для синтеза NO является L-аргинин (рис. 2).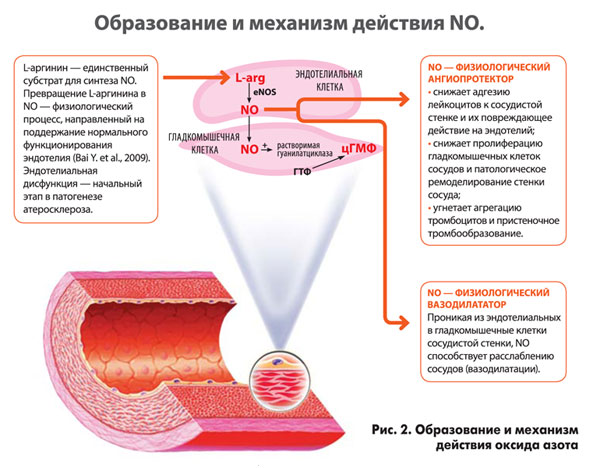
Следует отметить, что система синтеза и высвобождения NO эндотелием обладает значительными резервными возможностями, поэтому первой реакцией на неадекватное повышение сосудистого тонуса становится увеличение продукции оксида азота. Однако в последующем хроническая потребность в постоянном стимулировании синтеза NO приводит к истощению резерва L-аргинина, восполнить который призван новый класс эндотелиопротекторов – донаторов оксида азота. Представителем данного класса препаратов является Тивортин® – препарат, содержащий оптимальную суточную концентрацию L-аргинина.
Таким образом, коррекция ЭД должна быть рутинной и обязательной частью терапевтических и профилактических программ при лечении пациентов с сердечно-сосудистой патологией.
Имеющийся арсенал лекарственных средств и немедикаментозных методов лечения уже сегодня позволяет эффективно корригировать ЭД.
Материалы напечатаны в Медична газета «Здоров’я України» №7 • 2010 р.
Кардіопротекторний ефект донатора оксиду азоту в пацієнтів з артеріальною гіпертензією
Резюме: Останнє десятиліття ознаменувалося інтенсивним розвитком фундаментальних та клінічних досліджень щодо ролі судинного ендотелію в ґенезі серцево-судинних захворювань (ССЗ). Сьогодні увага дослідників прикута до вивчення ролі дисфункції ендотелію (ДЕ) в патогенезі ССЗ, а також до пошуку способів її ефективної корекції. В статті наводяться дані міжнародних і українських публікацій щодо можливого кардіопротекторного ефекту донатора оксиду азоту […]
ЗДОРОВ’Я НЕФРОНА — ЗАПОРУКА СТАБІЛЬНОГО АРТЕРІАЛЬНОГО ТИСКУ
Хронічна хвороба нирок (ХХН) є однією з найбільш поширених проблем у системі охорони здоров’я з тяжкими соціальними й економічними наслідками. Ця гетерогенна група захворювань об’єднує будь-які порушення нормальної структури й функції нирок з подальшим виникненням ниркових і позаниркових розладів, що мають несприятливий вплив на більшість систем організму. Важливою проблемою в усьому світі на сьогодні є […]
