ОПТИМИЗАЦИЯ ПОДГОТОВКИ МОРФОФУНКЦИОНАЛЬНОЙ СТРУКТУРЫ ЭНДОМЕТРИЯ В ПРОГРАММАХ ВРТ
ОПТИМИЗАЦИЯ ПОДГОТОВКИ МОРФОФУНКЦИОНАЛЬНОЙ СТРУКТУРЫ ЭНДОМЕТРИЯ В ПРОГРАММАХ ВРТ
Репродуктивная медицина – особое направление медико-биологических знаний, планирования семьи, безопасного материнства и сексуального здоровья. Она вобрала в себя достижения многих наук и ею изучаются все аспекты репродуктивного здоровья человека с момента рождения и до глубокой старости. Современная репродуктивная медицина – медицина семьи в целом. Одна из актуальных медико-социальных проблем в наши дни – бесплодный брак. В последние десятилетия в развитых странах мира растет количество супружеских пар,столкнувшихся с этой проблемой [1,4,7].
Проблема бесплодия — глобальная, выходящая за рамки государственной и требующая индивидуального похода к супружеской паре. Ведущее место в структуре женского бесплодия занимает трубно-перитонеальная форма [3,9]. Проблема лечения больных, страдающих бесплодием трубно-перитонеального генеза, сохраняет свою актуальность, несмотря на существенный прогресс в инструментальном исполнении и широкий арсенал медикаментозных средств [5–7,11]. Кроме того, при бесплодии трубно-перитонеального генеза чаще всего встречается нарушение морфофункционального слоя эндометрия, развивающегося на фоне длительных хронических заболеваний органов малого таза и ранее проведенных различных вариантов лечения.
В условиях постоянного присутствия повреждающего агента в ткани не происходит завершения заключительной фазы воспаления (регенерации), нарушается тканевой гомеостаз и формируется целый каскад вторичных повреждений. Нарушение микроциркуляции в эндометрии приводит к ишемии и гипоксии ткани, активированные макрофаги в очаге воспаления выступают источником активных радикалов кислорода и перекиси водорода и запускают процесс перекисного окисления липидов и повреждение клеточных мембран.
Основным диагностическим критерием оценки состояния эндометрия при 2D ТВЭ является его толщина (Kovach P. еtal., 2003). Эхографическая толщина эндометрия отображает степень подготовки эндометрия эстрогенами. Доказано, что в случаях, когда толщина эндометрия менее 5 мм, имплантация не происходит и перенос эмбрионов лучше не проводить (Zaidi J. etal., 1995). В литературе описаны лишь единичные случаи наступления беременности, когда толщина эндометрия в циклах ЭКО была менее 5 мм (Sundstrom P., 1998).
Толщина эндометрия в пределах 5–7 мм является субоптимальной, то есть имплантация возможна, но ее вероятность низка по сравнению с толщиной эндометрия выше 7 мм. Идеальной толщиной эндометрия считается 9–12 мм (Zaidi J. etal., 1995).
В последние годы с целью мониторинга циклов ВРТ активно используют допплерографию. Кровоток в маточных артериях был впервые использован как маркер рецептивности эндометрия (Goswamy et al., 1998). Позднее в работах многочисленных авторов была доказана коррелятивная связь маточного и яичникового кровотока с фолликулогенезом и результативностью циклов ВРТ (Федорова Е.В., 2002).Для повышения информативности УЗИ рекомендуется проведение оценки допплерометрических показателей кровотока сосудов матки с использованием новых технологий, в частности цветовой допплерометрии, трехмерной визуализации и ЗD-допплерометрии.
В последнее время в литературных источниках описано эффективное применение донаторов оксида азота в лечебном цикле перед циклом с использованием ВРТ. На рынке Украины существует препарат с активным метаболическим (эндотелиопротекторным) действием – Тивортин (ООО «Юрия-Фарм», Украина).
Активное действующее вещество в составе Тивортина – аминокислота аргинин — относится к разряду условно незаменимых, то есть частично синтезируемых в организме, но в количестве, не покрывающем суточной потребности в ней человека, что требует регулярного дополнительного поступления аргинина.
Аргинин – важный протектор и регулятор внутриклеточных обменных процессов, оказывающий влияние на различные жизненно важные функции органов и тканей и защищающий их в критических ситуациях. Эта аминокислота оказывает антиоксидантное, цитопротекторное, антигипоксическое, дезинтоксикационное, антиастеническое и мембрано-стабилизирующее действие, участвует в реакциях образования энергетического субстрата и в значительной степени поддерживает гормональный баланс в организме женщины. Аргинин способствует повышению содержания в плазме инсулина, а также глюкагона, пролактина и соматотропина. Он играет определенную роль в образовании в организме полиаминов и аминокислоты пралина, включается в реакции деполяризации клеточных мембран, процессы фибринолиза и сперматогенеза.
Аргинин является субстратом NO-синтаз в синтезе оксидаазота NO, являющегося локальным тканевым гормоном с множественными эффектами— от провоспалительного до сосудистых эффектов и стимуляции ангиогенеза. Усиленное образование NO ведет к дилатации периферических сосудов и снижению общего периферического сопротивления, что способствует снижению артериального давления и уменьшению кислородного голодания различных тканей, в первую очередь миокардиальной. Также происходит активизация гуанилатциклазы и повышение количества циклического ГМФ (гуанОзинмонофосфата) в эндотелиоцитах, снижение адгезии и агрегации тромбоцитов и лейкоцитов, синтез адгезивных протеинов МСР-1 и VCAM-1, что способствуют предотвращению образования атеросклеротических бляшек. Препарат угнетает образование эндотелина – вещества, оказывающего мощное вазоконстрикторное действие и являющегося стимулятором деления гладкомышечных клеток стенки сосудов.
Аргинин является донором оксида азота, открытие биологических эффектов которого было удостоено Нобелевской премии в медицине.
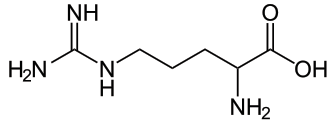
Рис.1 Химическая формула аргинина
В физиологических условиях синтез NO из L-аргинина происходит спомощью ферментов NO-синтаз (NO-synthase— NOS), вторым продуктом реакции является L-цитруллин.
NOS— единственный известный на данный момент фермент, использующий в этом процессе
одновременно 5 кофакторов/простетических групп (флавинадениндинуклеотид, флавинмононуклеотид, гем, тетрагидробиоптерин и кальций/кальмодулин), являясь таким образом одним из наиболее регулируемых в природе ферментом (Bryan N.S. etal., 2009).
Существует несколько изоформ NOS, названных по типу клеток, где они были впервые выделены — нейрональная (nNOS, NOS I), эндотелиальная (eNOS, NOS III) и макрофагальная (iNOS, NOS II).еNOS и nNOS постоянно присутствуют в соответствующих клетках, то есть являются конститутивно экспрессируемыми. еNOS отводится ведущая роль в обеспечении постоянного базисного уровня NO, который ассоциируют с реализацией механизмов локальной эндотелиальной цитопротекции и поддержанием сосудистого гомеостаза, физиологической регуляцией артериального давления (АД). Кроме того, еNOS выявлена и в других клетках и тканях, например в кардиомиоцитах, эритроцитах, мегакариоцитах, тромбоцитах (Гуревич М.А., СтуровН.В., 2006; BögerR.H., 2007; GkaliagkousiE. Et al., 2007).
Из желудочно-кишечного тракта, при приеме раствора перорально, аргинин абсорбируется за 15-20 минут, проникает через гистогематический барьер и относительно равномерно распределяется в тканях и органах. Преимущественный путь его выведения – через почки с мочой.
Аргинин является аминокислотой, активным и разносторонним клеточным регулятором жизненно важных функций организма, обладает протекторным эффектом. Тивортин оказывает антигипоксическую, цитопротекторную, мембраностабилизирующую, антирадикальную, антиоксидантную, дезинтоксикационную активность, является активным регулятором промежуточного обмена и процессов энергообеспечения, участвует в поддержке гормонального баланса. Аргинин участвует в цикле синтеза мочевины в печени. Обеспечивает гепатопротекторное действие, оказывает кислотообразующее действие и способствует коррекции кислотно-щелочного баланса.
Тивортин является субстратом для NО-синтазы, активирует гуанилатциклазу и повышает уровень циклического гуанидинмонофосфата в эндотелии сосудов, уменьшает активацию и адгезию лейкоцитов и тромбоцитов к эндотелию сосудов, предотвращает образование и развитие атеросклеротических бляшек, угнетает синтез эндотелина-1, который является мощным вазоконстриктором и стимулятором пролиферации и миграции гладких миоцитов сосудистой стенки. Тивортин подавляет синтез эндогенного стимулятора оксидативного стресса, стимулирует деятельность вилочковой железы, регулирует содержание глюкозы в крови во время физической нагрузки.
Целью нашего исследования явилось изучение эффективности использования препарата Тивортин, содержащего аргинин, который является субстратом для синтеза оксида азота, в циклах ВРТ с целью восстановления имплантационной способности эндометрия и повышению эффективности ВРТ.
Материалы и методы исследования
Данное исследование проводилось в отделении планирования семьи и ВРТ с кабинетом эндокринной гинекологии и дневным стационаром Клиники репродуктивных технологий Украинского государственного института репродуктологии НМАПО имени П.Л. Шупика.
На основании данных анамнеза, предварительного клинического обследования были отобраны в І (основную) группу исследования 31 пациентка с бесплодием, обусловленным перенесенными ХВЗОМТ (неспецифический хронический эндометрит), и неудачными попытками ВРТ в анамнезе.
Во II (контрольную) группу вошли 40 пациенток с бесплодием, также обусловленным перенесенными ХВЗОМТ (неспецифический хронический эндометрит) и неудачными попытками ВРТ в анамнезе.
Средний возраст пациенток составил 32,5 ± 3,1 года. Первичное бесплодие было выявлено у 15 (48,4%) пациенток. Лечение бесплодия методами ВРТ до настоящего момента проходили все пациентки данной группы (100%), из них 12 женщин (38,7%) — 2 попытки, одна (3,2%) — 3 попытки, три (9,7%) женщины — 4 попытки с отрицательным результатом.
Пациентки обеих групп были обследованы согласно алгоритмам обследования больных с бесплодием, которые регламентированы Приказом МЗ Украины № 582 от 15.12.2003 г. «Об утверждении клинических протоколов по акушерской и гинекологической помощи», раздел «Тактика ведения женщин с бесплодием» и инструкцией по применению вспомогательных репродуктивных технологий (Приказ № 787 от 09.09.2013 г. «Об утверждении Порядка применения вспомогательных репродуктивных технологий в Украине»).
Пациенткам обеих групп на первом этапе была назначена стандартная противовоспалительная терапия, содержащая антибиотики широкого спектра действия, антианаэробные препараты и иммуномодуляторы.
На втором этапе комплексной терапии пациенткам основной группы назначали препарат Тивортин (ООО «Юрия-Фарм», Украина),содержащий аргинин, с целью восстановления морфофункционального потенциала ткани эндометрия и устранения последствий вторичного повреждения, а именно: последствий ацидоза, восстановление гемодинамики и активности рецептивного аппарата эндометрия. Тивортин назначали сначала менструального цикла в/в по 4,2 грамма (100 мл) в течении 10 дней с последующим переходом на пероральный прием по 5 мл 4 раза в день до окончания менструального цикла.
Пациенткам второй группы с целью метаболической терапии назначали витаминотерапию (аскорбиновая кислота+витамин Е) в І и ІІ фазы менструального цикла соответственно.
Результаты исследования и их обсуждение
Характеристики клинической картины больных в обеих группах были однородными.
Было проведено наблюдение и обследование 71 пациентки с бесплодием, имеющих от 2 до 5 безуспешных циклов ВРТ в анамнезе при переносе в полость матки эмбрионов «хорошего» качества. В анамнезе у всех пациенток отмечен перенесенный эндометрит различной этиологии.
Методикой контроля эффективности лечения являлось ультразвуковое сканирование органов малого таза с допплерометрией сосудов матки. Результаты УЗИ сопоставляли с данными гистологического и цитологического исследований эндометрия. В обеих группах исследования после проведенного лечения предложенным нами методоми после стандартной комплексной терапии толщина, эхогенность, эхоструктура эндометрия соответствовала норме. Ультразвуковую анатомию эндометрия рассматривали на 5-7 и 17-21 дни менструального цикла. В фазу ранней пролиферации (5-7дни цикла) эндометрий имел относительно низкую эхогенность и однородную эхоструктуру. Толщина колебалась в пределах 3-6 мм, составляя в среднем 5 мм. В фазу средней секреции (17-21 дни) эндометрий достигал максимальной толщины — в среднем 11 мм (колебания 10-13 мм). Эхогенность еще более повышалась, гиперэхогенная линия в центре визуализировалась плохо либо невизуализировалась вообще.
В предыдущих лечебных циклах толщина эндометрия у наблюдаемых пациенток на момент ПЭ не превышала 3-5 мм, и были выраженные нарушения показателей маточной гемодинамики. Эти пациентки были толерантны к ранее проводимой общепринятой подготовительной терапии. После проведенного лечения у пациенток основной группы на момент ПЭ толщина эндометрия составляла 8-10 мм. При допплерометрическом исследовании отмечено снижение индекса резистентности в маточных и мелких радиальных артериях и повышение конечной диастолической скорости кровотока. Частота наступления беременности у пациенток основной группы составила 48%, тогда как у пациенток контрольной группы – 24% (рис. 2).
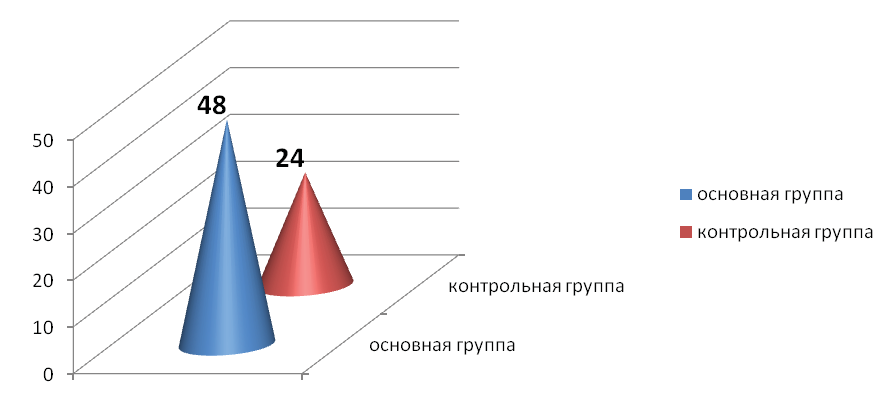
Рис. 2 Сравнение эффективности проведенной терапии у пациенток основной
и контрольной групп.
Выводы
Наше исследование показало, что использование в комплексной терапии перед циклами ВРТ препарата Тивортин (ООО «Юрия-Фарм», Украина), содержащего аргинин,улучшает маточный кровоток и восстанавливает морфофункциональное состояние эндометрия, достоверно увеличивает имплантационную возможность эндометрия, что в свою очередь повышает частоту наступления беременностей.
Кардиопротекторный эффект донатора оксида азота у пациентов с артериальной гипертензией
Резюме: Последнее десятилетие ознаменовалось интенсивным развитием фундаментальных и клинических исследований роли сосудистого эндотелия в генезе сердечно-сосудистых заболеваний (ССЗ). Сегодня внимание исследователей приковано к изучению роли дисфункции эндотелия (ДЭ) в патогенезе ССЗ, а также к поиску способов ее эффективной коррекции. В статье приводятся данные международных и украинских публикаций о возможном кардиопротекторном эффекте донатора оксида азота у […]
ЗДОРОВЬЕ НЕФРОНА — ЗАЛОГ СТАБИЛЬНОГО АРТЕРИАЛЬНОГО ДАВЛЕНИЯ
Резюме: Хроническая болезнь почек является одним из наиболее распространенных заболеваний в мире. Наряду с повреждением собственно почки заболевание связано с большими рисками со стороны сердечно-сосудистой, эндокринной и других систем организма. Обзор представляет последние взгляды на проблему и данные исследований, а также современные терапевтические решения для всестороннего лечения заболевания и проведения патогенетически обоснованной коррекции волюмодинамики. Рассмотренный […]
